|
2. ЛІТЕРАТУРНИЙ ОГЛЯД
2.1 КОРОЗІЯ
<>Під корозією розуміють таку взаємодію між металом і
середовищем, що призводить до погіршення функціональних властивостей металу,
середовища або їхньої системи [5].
Більшість
металів, від моменту виплавки піддаються дії корозійних факторів оточуючого
середовища. Вироби з чавуну та сталі кородують скрізь, де б вони не
знаходилися: у повітрі, в землі чи у воді [13].
В залежності від хімічного складу середовища, умов
протікання та виду корозійних руйнуваннь вирізняють близько 40 видів корозії:
атмосферну, газову, контактну, біокорозію, щілинну, корозію при тертті та ін.[10-16].
Вузли і деталі автомобілів, сільскогосподарської,
будівельної і військової техніки, верстати, інші металовироби під час виготовлення, транспортування,
збереження, періодичної або постійної експлуатації піддаються практично усім
видам корозії, з яких найбільш пошириною є атмосферна корозія [5]<>.
Атмосферна
корозія, як умовний
вид корозії, є сукупністтю корозійних процесів, що відбуваються на поверхні металів
при їх контакті з атмосферою. Під час зберігання та транспортування
металовиробів, поверхня останніх може контактувати з частинками грунту, пилу,
золем сольових розчинів тощо. В результаті опадів або атмосферної вологи, на
поверхні металу утворюються адсорбційна або конденсаційна плівки вологи, які
при взаємодії з кислотними оксидами та солями атмосфери утворюють електроліти
[13, 14, 17].
Крім
того, наявність приповерхневої плівки вологи сприяє розвитку мікроорганізмів –
біологічних активаторів корозії [<>18].
Таким
чином велика різноманітть чинників атмосферної корозії здатна викливати всі
різновиди пошкодженнь і призводить до перебігу атмосферної корозії в
найрізноманітніших умовах: при транспортуванні та зберіганні металовиробів на
відкритих площадках, під навісом, в опалюваних і неопалюваних приміщеннях, при
експлуатації [5].
Для успішної боротьби з атмосферною корозією необхідно
встановити природу, складові, характер, механізм, умови та основні чинники
перебігу процесів атмосферної корозії.
Природа та складові атмосферної корозії. За своєю природою
корозія як взаємодія корозійних агентів середовища з металом, є гетерогенним
процесом [19].
Атмосферна
корозії включає не менш трьох складових, руйнівний цикл яких можна розглядати
як його циклічні стадії в наступному порядку[19]:
<>1) Підвід корозійних
агентів у зону реакції до поверхні металу;
<>2) Безпосереднє
окиснення металу, що призводить до утворення продуктів реакції;
<>3) Відвід продуктів
реакції з поверхні металу.
Загальна швидкість корозійного процесу
визначається стадією з мінімальною інтенсивністтю. В свою чергу швидкість
корозійного процесу на кожній із стадій залежить від хімічної природи металу,
середовища, корозійних агентів, а також температури, тиску, освітлення,
механічного впливу тощо.
Інтенсивність підводу реагентів до поверхні
металу визначається швидкісттю дифузії та концентрацією корозійних агентів у
середовищі. Підведення корозійних агентів до поверхні металу на початковому
етапі тісно пов¢язане з інтенсивністтю руйнування первинних оксидних
плівок на металі, а також з інтенсивністтю відводу продуктів корозії.
Інтенсивність відводу продуктів корозії
визначається їх взаємодією із середовищем. У випадку активної взаємодії
продуктів корозії з середовищем швидкість відводу продуктів корозії є
максимальною [20].
Кінетичні
особливості атмосферної корозії. <>В залежності від ефективності відводу продуктів корозії
виділяють три періоди їх накопичення: індукційний, перехідний, стаціонарний [13, 21]
В
індукційному періоді йде руйнування первинної оксидної
плівки на металі, у перехідному - формування проміжних і кінцевих продуктів. У
стаціонарному періоді встановлюється така швидкість корозії, при якій кількість
продуктів, що утворюються, майже зрівнюється з кількістю відведених (наприклад,
внаслідок розчинення або змивання дощовою водою) [16].
В залежності від здатності середовища розчиняти
продукти корозії розрізняють три типи розвитку корозійних процесів у часі (мал.
12.5) [13].
●
Перший тип характеризується швидким майже повним припиненням корозії за
короткий час (мал. 2.1 крива 1), внаслідок утворення на поверхні металу
щільної, непроникної для корозійних агентів середовища, пасиваційної плівки з
продуктів корозії.
●
Другому типу відповідає порівняно швидкий початковий корозійний процес з наступним
нарощуванням захисного шару продуктів, що неруйнується або частково руйнується
у середовищі або має пори через які можливий доступ корозійних агентів до
поверхні металу (мал. 2.1 крива 2).
● Третій тип
характеризується утворенням продуктів корозії, які майже не мають захисного
ефекту і легко руйнуються. Окиснення цих металів підкорюється лінійному
законові (мал. 2.1 крива 3).
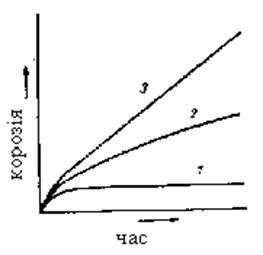
мал. 2.1
Швидкість корозії в залежності від характеру
утворюваних продуктів корозії.
1- група хрому; 2- група міді; 3-група цинку.
<>Механізми, чинники<> та умови атмосферної корозії. Друга стадія процесу корозії (безпосередня
взаємодія корозійних агентів середовища) може відбуватися лише за двома
механізмами: хімічним та електрохімічним. Хімічна корозія проходить за законами
суто хімічної кінетики гетерогенних реакцій [5, 13-16]. Обов¢язковою умовою
проходження корозії за хімічним механізмом є зменшення енергії Гіббса системи
(ΔG<0)
у результаті хімічної реакції [22]. Чинниками атмосферної
корозії , що проходить за хімічним механізмом можуть бути деякі гази: Н2S, SO2, SO3 , NO2 і ін. [13- 15]
Під час хімічної корозії електрони атомів металу,
долають відносно невелику відстань, переходячи до структури атомів більш
електронегативної речовини, що не призводить до виникненням електричного
струму. Така корозія може спостерігатись в неелектролітах чи в сухій атмосфері [14-16, 19]. Електрохімічна корозія
характеризується протіканням електричного струму і проходить за законами
електрохімічної кінетики. У випадку електрохімічної корозії електрони атомів
металу долають велику відстань, порівняно з розмірами самих атомів. Для
перебігу електрохімічної корозії необхідна наявність електропровідного
середовища, що містить речовину яка здатна відновлюватись [14, 15]. Речовина, яка під час
електрохімічного процесу корозії відновлюється, окислюючи при цьому метал
носить назву деполяризатора [23, 24]. Для проходження
електрохімічного процесу корозії рівноважний електродний потенціал металу
повинен бути меньшим за рівноважний електродний потенціал деполяризатора.
Ед – Ем> 0
Загальна реакція електрохімічної корозії ділиться на два процеси,
що протікають самостійно: анодний (перехід металу в розчин у вигляді
гідратованих іонів) і катодний (асиміляція надлишкових електронів, які
з'явилися в металі в результаті анодного процесу, будь-якими деполяризаторами
— атомами, іонами чи молекулами розчину, які можуть відновлюватись на катоді).
Dox + ne = Dredox n- катод
Me –ne = Men+ анод
Dox + Me = Dredox n- + Men+ сумарно
Збудниками (деполяризаторами) в
процесах атмосферної корозії є присутні в повітрі: кисень, вуглекислий газ,
сірководень, сірчистий газ, деякі неорганічні та органічні кислоти (соляна,
сірчана, сірчиста, мурашина і ін.) [5, 10, 14].
До умов, що визначають механізм перебігу корозії
належать: природа реагуючих речовин, температура та її перепад, рівень
вологості атмосфери, присутність легко дисоціюючих речовин (кислот, солей,
лугів, деяких газів), активність мікроорганізмів [7, 14-20]. Найважливішою умовою
домінування електрохімічних процесів над хімічними є наявність на поверхні
металів електропровідної плівки вологи або електроліту [10, 13-16].
Зазвичай, незахищені металовироби, що
зберігаються у приміщеннях, під навісами або на площадках вкриті шаром вологи.
В залежності від ступеня зволоження кородуючої поверхні
атмосферну корозію поділяють на три види [19]:
- волога, коли волога плівка (від 1 мк до 1 мм) утворюється внаслідок краплинної конденсації (вона спостерігається, коли волога
безпосередньо потрапляє на поверхню металу від дощу, бризок, снігу або при
відносній вологості повітря близький 100%);
- конденсаційна, утворюється при відносній вологості повітря нижче
100% і товщині плівки від 100А до 1 мк (якщо вологість нижча 100%,
можлива капілярна, хімічна і адсорбційна конденсація) ;
- суха, коли шар вологи зовсім відсутній на поверхні металу при
товщині плівки меншій 100А.
Волога і конденсаційна атмосферна корозія відбуваються під
видимою плівкою вологи, і при відносній вологості нижчій 100% розглядаються як
корозія під плівкою електроліту, оскільки у сконденсованій волозі завжди є
розчинені солі, кислоти, луги. Процеси, що розвиваються в цих випадках, мають
електрохімічну природу та високу інтенсивність [25, 26].
Як хімічні так і електрохімічні корозійні процеси пришвидшуються
при наявності в атмосфері сполук, що містять сірку (SO2, SО3, H2S), а також домішки NН3, NO2 і Сl2. Реагуючи з водою, дані
сполуки утворюють речовини, що пошкоджують оксидні захисні плівки на металах,
перетворюючи їх на розчинні у атмосферній волозі солі [13].
Умови перебігу корозійних процесів температура та її перепад,
вологість, кількість опадів, присутність легко дисоціюючих речовин, кислот,
солей, лугів, наявність в атмосфері корозійно активних газів, активність
організмів багато в чому залежать від географічної та кліматичної зони в яких
проходить процес.
Розрізняють континентальну і морську атмосферну корозію [13,
24–27]. В свою чергу в континентальній атмосфері виділяють сільскі, промислові
(індустріальні), міські, та тропічні умови перебігу корозії. [13, 20]
Континентальна
атмосферна корозія. Континентальна атмосферна корозія металів підсилюється через
присутність в атмосфері міст і промислових зон сірковмісних сполук: сірчистого
і сірчаного ангідридів, сірководню. При цьому в присутності вологи утворюються
кислоти, що руйнують наявні на металах природні захисні плівки і прискорюють
корозію, оскільки продукти корозії легкорозчинні у воді [13, 28].
SO3+ H2O = H2SO4
SO2+H2O = H2SO3
MenOm + mH2SO3 =
n Me(SO3)m + m H2O
MenOm + mH2SO4 =
n Me(SO4)m + m H2O
MenOm+H2S = MenSm+
mH2O
Морська
атмосферна корозія. У морській атмосфері корозія сильніша, ніж у континентальній,
так як в морській атмосфері міститься велика кількість солей, які сприяють
утворенню електроліту на поверхні металу, а в процесі корозії руйнують захині
оксидні прошарки [13].
Корозійні процеси на металах також залежить і від пори року.
Навесні корозія металів, як правило, посилюється у зв'язку з таненням снігу, що
концентрує за зиму велику кількість корозійно-активних промислових домішок.
Осіння погода теж сприяє інтенсифікації корозії, так як дощова вода може
містити суттєву кількість (до 200 мг/л) мінеральних солей [19, 25–29].
Таким чином атмосферна
корозія може проходити за хімічним та електрохімічним механізмом, що
визначається природою кородуючого металу та умовами навколишнього середовища. У
природних умовах домінуючим механізмом атмосферної корозії є електрохімічний.
Основною причиною домінантності, а також фактором виникнення електрохімічної
корозії є наявність на поверхні металу конденсаційної або адсорбційної плівки
вологи.
Забрудненість повітря
корозійноактивними газами, парами кислот, дустом солей, пилом, мікроорганізмами
перетворює плівку вологи, на поверхні металу, в електроліт, що пришвидшує
корозію як за рахунок введення деполяризаторів так і за рахунок зменшення
пасиваційної властивості продуктів окиснення металу. Волога в корозійних
процесах відіграє роль електроліту, тобто середовища, яке здатне підводити
корозійні агенти до металевої поверхні та розчиняти пасиваційні плівки на
поверхні металу.
|



